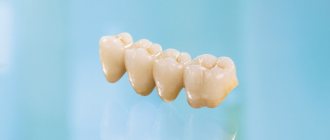
Остеопластика в стоматологии – наращивание костной ткани, необходимой для удачной имплантации. После того, как человеку удалили зуб, твердая ткань имеет свойство рассасываться, а новый искусственный зуб должен надежно держаться в челюсти. Наращивание кости для имплантации зубов успешно решает эту проблему, но требует дополнительных затрат и больше времени (чем, например, при одномоментной имплантации, когда объема ткани достаточно).
Остеопластика – что это такое, и зачем она нужна?
При внедрении титанового корня очень важно, чтобы он со всех сторон был окружен костью. Если есть дефицит ткани, то титановый штифт будет отторгаться. Более того, если корень установлен в верхнюю челюсть, есть риск задевания верхнечелюстных пазух, что может привести к серьезным ЛОР-заболеваниям. Также при недостатке кости имплантат будет расшатываться, опустится ниже десны, что скажется на эстетике протеза и общей картине.
Остеопластика рекомендована в таких случаях:
- если необходимо установить корень в зону, где свой зуб был удален несколько лет (или месяцев) тому назад;
- если у пациента анатомически большие гайморовые пазухи;
- когда физиологически у человека минимальный объем твердой ткани.
Операция не выполняется, если:
- у пациента хронические ЛОР-заболевания (гаймориты, синуситы, риниты);
- нехватка кальция в организме;
- есть патологии в строении дыхательной системы;
- онкология;
- полипы и другие образования в носу;
- сахарный диабет.
Также остеопластика не выполняется беременным и кормящим женщинам. В остальном, операция делается относительно быстро и с гарантией.
Во многих случаях пациентам перед операцией рекомендуют пропить курс гормональных препаратов и антибиотиков, чтобы нейтрализовать отечные состояния и возможные воспаления.
Вместо пролога. Что такое биоматериалы?
С точки зрения толкового словаря, под биоматериалами подразумеваются любые чужеродные вещества и объекты, внедряемые в организм и дополняемые его структурно или/и функционально, и использующиеся в медицинских целях. То есть, биоматериалами можно назвать искусственные клапаны сердца, эндопротезы, имплантаты, в т. ч. дентальные, металлоконструкции, применяемые при остеосинтезе, гемостатические средства, зубные протезы, коронки, вкладки, пломбы и т. д. И наоборот, сережки для пирсинга, краски для татуировок, всякие страшные штуки для боди-моддинга к биоматериалам, в правильном их понимании, не относятся.
То, что мы используем для “наращивания костной ткани”, было бы правильнее назвать “биоматериалами для регенеративной хирургии”, что конкретизирует и объясняет их назначение. В общих чертах, современный стоматологический рынок предлагает нам три категории таких материалов – остеографты, барьерные мембраны и мукографты:
Чуть позже, мы подробно рассмотрим каждую из этих категорий.
Говорить о показаниях и противопоказаниях к использованию биоматериалов с точки зрения пациента достаточно сложно, поэтому их использование в ходе тех или иных остеопластических операций – вопрос, относящийся больше к конкретной методике, нежели к самому материалу. Поэтому мы будем рассматривать его в статьях, посвященных определенным методикам остеопластики. То есть, скоро.
Но, в целом, уважаемые друзья, вам нужно знать следующее:
– использование биоматериалов – это всегда компромисс, вынужденная мера.
Да, теоретически и практически, мы могли бы обходиться без них. И тому есть масса примеров:
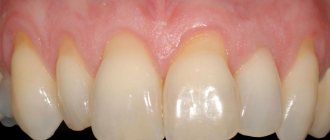
уточню, что на двух правых снимках – временная коронка на установленном имплантате. Биоматериалы для остеопластики в данном клиническом случае не применялись.
Но в таких случаях мы сталкиваемся с проблемой – если нам необходимо возместить атрофическую утрату кости или слизистой оболочки, то её необходимо где-то взять. И нередко процесс получения аутотрансплантата (т. е., собственного фрагмента тканей для пересадки) увеличивает травматичность, сложность и продолжительность хирургического вмешательства. А иногда вообще является отдельной хирургической операцией со всеми вытекающими: повышаются риски осложнений и снижается безопасность хирургического лечения. Совершенно логичным выглядит желание всего этого избежать, заменив аутотрансплантат чем-то “искусственным”.
– ни один из существующих биоматериалов не улучшает качество регенерирующих тканей.
Это микроскопная фотография того, что получается после остеопластики с использованием биоматериалов.
Если мы говорим, к примеру, о “наращивании костной ткани”, то ни один из остеографтов, используемых в современной хирургической практике, не делает кость крепче, прочнее, красивее и т. д. Более того, то, что мы получаем в результате использования “искусственных заменителей кости”, сложно назвать костью в биологическом смысле – скорее, это костная мозоль с включением частиц биоматериала(как на микроскопной картинке выше), её свойства и структура сильно отличаются от нормальной здоровой костной ткани. Если уж говорить совсем серьезно, то использование графтов “ухудшает” качество тканей. Но мы вынуждены идти на этот компромисс, чтобы восполнить их объем и, соответственно, создать условия для нормальной имплантологической реабилитации.
– не существует биоматериалов, ускоряющих регенерацию тканей.
Я бы даже сказал больше – от марки, производителя или страны происхождения биоматериала мало, что зависит. Все существующие в мире графты и барьерные мембраны работают одинаково, по одним и тем же биологическим законам. Категорически неправильно утверждать, что “этот материал работает лучше, чем этот” или “вот этот хороший, а этот – полное говно!”. Безусловно, биоматериалы отличаются между собой целым рядом свойств, и сегодня мы с вами обязательно поговорим об этих свойствах.
– у каждой из категорий биоматериалов есть своё назначение и чётко прописанная функция.
Прямо как на этой картинке:
Использовать биоматериалы не по назначению – это, как минимум, серьезно рисковать результатом. Например, мы можем попытаться с использовать гемостатическую губку для заполнения субантрального пространства при синуслифтинге. И, возможно, мы даже получим хороший результат. Но, только слово “возможно” меня лично очень смущает. В хирургии использование этого слова должно быть сведено к минимуму.
– использование биоматериалов должно быть обоснованным и понятным, прежде всего, вам.
“Сюда засунем, здесь приколотим” … иными словами, использование графтов и барьерных мембран, – это всегда отличный способ завысить стоимость лечения или искусственно усложнить предстоящую операцию. И действительно, установленные имплантаты можно пересчитать, по контрольным снимкам легко определяется их марка и модель, а вот определить объем де-факто использованного при синуслифтинге графта или размер установленной барьерной мембраны (да и вообще, наличие этой самой мембраны) не так уж и просто. Если вы по каким-то причинам не понимаете, для чего необходимо использование биоматериалов в вашем клиническом случае, значит, они не нужны. Об их применении в различных клинических ситуациях мы поговорим в последующих статьях, когда будем изучать каждый из существующих методов остеопластики. Ну и, после операции имеет смысл “свериться” с реальным расходом биоматериалов – все графты и барьерные мембраны используемые в современной хирургии, имеют специальные наклейки с указанием их параметров и серийных номеров, – одна наклейка остаётся в медицинской карте, вторая вклеивается в договор, на контрольный снимок или специальный бланк, которые передаются пациенту.
Наконец, последнее, от того не менее важное:
все существующие биоматериалы – одноразовые. Одна упаковка предназначена ТОЛЬКО для одной операции:
Это, собственно, значит, что во-первых, неиспользованные остатки биоматериалов нельзя повторно стерилизовать и использовать, а во-вторых, что отсутствие вышеуказанной наклейки говорит о том, что в вашем лечении, возможно, был использован “левый” материал или остатки с какой-то другой операции. Категорически не рекомендую на этом экономить, ибо правильно простерилизовать уже открытый материал в условиях обычной стоматологической клиники без потери его свойств невозможно.
В принципе, уважаемые друзья, знания вышеперечисленного вполне достаточно, чтобы понять, нужны ли недешевые, в общем-то, биоматериалы для наращивания костной ткани конкретно в вашем клиническом случае. На всякий случай напоминаю, что
если вы чего-то не понимаете, – значит вам это не нужно.
Вспомните, хотя бы, вот эту статью>>.
В рамках семинаров RegenerationDay by Geistlich, мне удаётся не только повысить чувство собственной важности, но и побеседовать с докторами из различных клиник, городов и регионов нашей страны. И я не могу не замечать зловредную тенденцию – чрезмерное злоупотребление биоматериалами, бестолковое желание затолкать их туда, где они, в принципе, не нужны. Многие в них видят какую-то панацею, некую “волшебную таблетку”, способную, если не гарантировать, то улучшить результат любой остеопластической операции. Увы, это не так.
В нашем стоматологическом центре делается очень много остеопластических операций – больше двухсот с начала года. При этом, расход биоматериалов относительно небольшой – они используются меньше, чем в половине случаев. Почему? Для ответа на этот вопрос нужно, как минимум, прочитать вот это>> или просто заглянуть к нам в клинику на консультацию.))
Типы костной ткани в стоматологии
- аллотрансплантат – синтетическая костная ткань в стоматологии, которая создается в лабораторных условиях. Это искусственный материал, который не всегда успешно приживается;
- внутриротовой аутотрансплантат – собственная костная ткань пациента, которая была взята из других зон ротовой полости. Например, из самой дальней части зубного ряда. Подобная процедура наращивания называется аутотрансплантацией;
- аллогенный костный материал в хирургической стоматологии – человеческая кость, донором которой является другой пациент. Высокие показатели приживаемости, но пациента может смущать, что этот материал взят из трупной кости, хоть и хранился в стерильной упаковке;
- ксенотрансплантат – заменитель костной ткани в современной стоматологии, материал животного происхождения. Заимствуется из костей крупного рогатого скота. Один из самых востребованных материалов для трансплантации, когда требуется большой объем твердой ткани;
- гранулы гидроксиапатита – искусственный костный трансплантат в стоматологии.
Определить конкретный вид костного материала в стоматологии вам поможет опытный стоматолог-имплантолог, который изучит состояние пациента, особенности ткани и оценит будущий фронт работ по восстановлению зубного ряда.
Кость представляет собой сложную материю, это сложный анизотропный неравномерный жизненный материал, обладающий упругими и вязкими свойствами, а также хорошей адаптивной функцией. Все превосходные свойства костей составляют неразрывное единство с их функциями.
Функции костей главным образом имеет две стороны: одна из них – это образование скелетной системы, используемой для поддержания тела человека и сохранения его нормальной формы, а также для защиты его внутренних органов. Скелет является частью тела, к которой крепятся мышцы и которая обеспечивает условия для их сокращения и движения тела. Скелет сам по себе выполняет адаптивную функцию путем последовательного изменения своей формы и структуры. Вторая сторона функции костей состоит в том, чтобы путем регулирования концентрации Ca2+ , H+ , HPO4+ в электролите крови поддерживать баланс минеральных веществ в теле человека, то есть функцию кроветворения, а также сохранения и обмена кальция и фосфора.
Форма и структура костей являются различными в зависимости от выполняемых ими функций. Разные части одной и той же кости вследствие своих функциональных различий имеют разную форму и структуру, например, диафиз бедренной кости и головка бедренной кости. Поэтому полное описание свойств, структуры и функций костного материала является важной и сложной задачей.
Структура костной ткани
«Ткань» представляет собой комбинированное образование, состоящее из особых однородных клеток и выполняющих определенную функцию. В костных тканях содержатся три компонента: клетки, волокна и костный матрикс. Ниже представлены характеристики каждого из них:
Клетки: В костных тканях существуют три вида клеток, это остеоциты, остеобласт и остеокласт. Эти три вида клеток взаимно превращаются и взаимно сочетаются друг с другом, поглощая старые кости и порождая новые кости.
Костные клетки находятся внутри костного матрикса, это основные клетки костей в нормальном состоянии, они имеют форму сплющенного эллипсоида. В костных тканях они обеспечивают обмен веществ для поддержания нормального состояния костей, а в особых условиях они могут превращаться в два других вида клеток.
Остеобласт имеет форму куба или карликового столбика, они представляют собой маленькие клеточные выступы, расположенные в довольно правильном порядке и имеют большое и круглое клеточное ядро. Они расположены в одном конце тела клетки, протоплазма имеет щелочные свойства, они могут образовывать межклеточное вещество из волокон и мукополисахаридных белков, а также из щелочной цитоплазмы. Это приводит к осаждению солей кальция в идее игловидных кристаллов, расположенных среди межклеточного вещества, которое затем окружается клетками остеобласта и постепенно превращается в остеобласт.
Остеокласт представляет собой многоядерные гигантские клетки, диаметр может достигать 30 – 100 µm, они чаще всего расположены на поверхности абсорбируемой костной ткани. Их цитоплазма имеет кислотный характер, внутри ее содержится кислотная фосфотаза, способная растворять костные неорганические соли и органические вещества, перенося или выбрасывая их в другие места, тем самым ослабляя или убирая костные ткани в данном месте.
Костный матрикс также называется межклеточным веществом, он содержит неорганические соли и органические вещества. Неорганические соли также называются неорганическими составными частями костей, их главным компонентом являются кристаллы гидроксильного апатита длиной около 20-40 nm и шириной около 3-6 nm. Они главным образом состоят из кальция, фосфорнокислых радикалов и гидроксильных групп, образующих [Ca10 (PO4) (OH)2], на поверхности которых находятся ионы Na+ , K+, Mg2+ и др. Неорганические соли составляют примерно65% от всего костного матрикса. Органические вещества в основном представлены мукополисахаридными белками, образующими коллагеновое волокно в кости. Кристаллы гидроксильного апатита располагаются рядами вдоль оси коллагеновых волокон. Коллагеновые волокна расположены неодинаково, в зависимости от неоднородного характера кости. В переплетающихся ретикулярных волокнах костей коллагеновые волокна связаны вместе, а в костях других типов они обычно расположены стройными рядами. Гидроксильный апатит соединяется вместе с коллагеновыми волокнами, что придает кости высокую прочность на сжатие.
Костные волокна в основном состоит из коллагенового волокна, поэтому оно называется костным коллагеновым волокном, пучки которого расположены послойно правильными рядами. Это волокно плотно соединено с неорганическими составными частями кости, образуя доскообразную структуру, поэтому оно называется костной пластинкой или ламеллярной костью. В одной и той же костной пластинке большая часть волокон расположена параллельно друг другу, а слои волокон в двух соседних пластинках переплетаются в одном направлении, и костные клетки зажаты между пластинками. Вследствие того, что костные пластинки расположены в разных направлениях, то костное вещество обладает довольно высокой прочностью и пластичностью, оно способно рационально воспринимать сжатие со всех направлений.
У взрослых людей костная ткань почти вся представлена в виде ламеллярной кости, и в зависимости от формы расположения костных пластинок и их пространственной структуры эта ткань подразделяется на плотную кость и губчатую кость. Плотная кость располагается на поверхностном слое ненормальной плоской кости и на диафизе длинной кости. Ее костное вещество плотное и прочное, а костные пластинки расположены в довольно правильном порядке и тесно соединены друг с другом, оставляя лишь небольшое пространство в некоторых местах для кровеносных сосудов и нервных каналов. Губчатая кость располагается в глубинной ее части, где пересекается множество трабекул, образуя сетку в виде пчелиных сот с разной величиной отверстий. Отверстия сот заполнены костным мозгом, кровеносными сосудами и нервами, а расположение трабекул совпадает с направлением силовых линий, поэтому хотя кость и рыхлая, но она в состоянии выдерживать довольно большую нагрузку. Кроме того, губчатая кость имеет огромную поверхностную площадь, поэтому она также называется Костю, имеющей форму морской губки. В качестве примера можно привести таз человека, средний объем которого составляет 40 см3 , а поверхность плотной кости в среднем составляет 80 см2 , тогда как поверхностная площадь губчатой кости достигает 1600 см2 .
Морфология кости
С точки зрения морфологии, размеры костей неодинаковы, их можно подразделить на длинные, короткие, плоские кости и кости неправильной формы. Длинные кости имеют форму трубки, средняя часть которых представляет собой диафиз, а оба конца – эпифиз. Эпифиз сравнительно толстый, имеет суставную поверхность, образованную вместе с соседними костями. Длинные кости главным образом располагаются на конечностях. Короткие кости имеют почти кубическую форму, чаще всего находятся в частях тела, испытывающих довольно значительное давление, и в то же время они должны быть подвижными, например, это кости запястья рук и кости предплюсны ног. Плоские кости имеют форму пластинок, они образуют стенки костных полостей и выполняют защитную роль для органов, находящихся внутри этих полостей, например, как кости черепа.
Кость состоит из костного вещества, костного мозга и надкостницы, а также имеет разветвленную сеть кровеносных сосудов и нервов, как показано на рисунке. Длинная бедренная кость состоит из диафиза и двух выпуклых эпифизарных концов. Поверхность каждого эпифизарного конца покрыта хрящом и образует гладкую суставную поверхность. Коэффициент трения в пространстве между хрящами в месте соединения сустава очень мал, он может быть ниже 0.0026. Это самый низкий известный показатель силы трения между твердыми телами, что позволяет хрящу и соседним костным тканям создать высокоэффективный сустав. Эпифизарная пластинка образована из кальцинированного хряща, соединенного с хрящом. Диафиз представляет собой полую кость, стенки которой образованы из плотной кости, которая является довольно толстой по всей ее длине и постепенно утончающейся к краям.
Костный мозг заполняет костномозговую полость и губчатую кость. У плода и у детей в костномозговой полости находится красный костный мозг, это важный орган кроветворения в человеческом организме. В зрелом возрасте мозг в костномозговой полости постепенно замещается жирами и образуется желтый костный мозг, который утрачивает способность к кроветворению, но в костном мозге по-прежнему имеется красный костный мозг, выполняющий эту функцию.
Надкостница представляет собой уплотненную соединительную ткань, тесно прилегающую к поверхности кости. Она содержит кровеносные сосуды и нервы, выполняющие питательную функцию. Внутри надкостницы находится большое количество остеобласта, обладающего высокой активностью, который в период роста и развития человека способен создавать кость и постепенно делать ее толще. Когда кость повреждается, остеобласт, находящийся в состоянии покоя внутри надкостницы, начинает активизироваться и превращается в костные клетки, что имеет важное значение для регенерации и восстановления кости.
Микроструктура кости
Костное вещество в диафизе большей частью представляет собой плотную кость, и лишь возле костномозговой полости имеется небольшое количество губчатой кости. В зависимости от расположения костных пластинок, плотная кость делится на три зоны, как показано на рисунке: кольцевидные пластинки, гаверсовы (Haversion) костные пластинки и межкостные пластинки.
Кольцевидные пластинки представляют собой пластинки, расположенные по окружности на внутренней и внешней стороне диафиза, и они подразделяются на внешние и внутренние кольцевидные пластинки. Внешние кольцевидные пластинки имеют от нескольких до более десятка слоев, они располагаются стройными рядами на внешней стороне диафиза, их поверхность покрыта надкостницей. Мелкие кровеносные сосуды в надкостнице пронизывают внешние кольцевидные пластинки и проникают вглубь костного вещества. Каналы для кровеносных сосудов, проходящие через внешние кольцевидные пластинки, называются фолькмановскими каналами (Volkmann’s Canal). Внутренние кольцевидные пластинки располагаются на поверхности костномозговой полости диафиза, они имеют небольшое количество слоев. Внутренние кольцевидные пластинки покрыты внутренней надкостницей, и через эти пластинки также проходят фолькмановские каналы, соединяющие мелкие кровеносные сосуды с сосудами костного мозга. Костные пластинки, концентрично расположенные между внутренними и внешними кольцевидными пластинками, называются гаверсовыми пластинками. Они имеют от нескольких до более десятка слоев, расположенных параллельно оси кости. В гаверсовых пластинках имеется один продольный маленький канал, называемый гаверсовым каналом, в котором находятся кровеносные сосуды, а также нервы и небольшое количество рыхлой соединительной ткани. Гаверсовы пластинки и гаверсовы каналы образуют гаверсову систему. Вследствие того, что в диафизе имеется большое число гаверсовых систем, эти системы называются остеонами (Osteon). Остеоны имеют цилиндрическую форму, их поверхность покрыта слоем цементина, в котором содержится большое количество неорганических составных частей кости, костного коллагенового волокна и крайне незначительное количество костного матрикса.
Межкостные пластинки представляют собой пластинки неправильной формы, расположенные между остеонами, в них нет гаверсовых каналов и кровеносных сосудов, они состоят из остаточных гаверсовых пластинок.
Внутрикостное кровообращение
В кости имеется система кровообращения, например, на рисунке показа модель кровообращения в плотной длинной кости. В диафизе есть главная питающая артерия и вены. В надкостнице нижней части кости имеется маленькое отверстие, через которое внутрь кости проходит питающая артерия. В костном мозге эта артерия разделяется на верхнюю и нижнюю ветви, каждая из которых в дальнейшем расходится на множество ответвлений, образующих на конечном участке капилляры, питающие ткани мозга и снабжающие питательными веществами плотную кость.
Кровеносные сосуды в конечной части эпифиза соединяются с питающей артерией, входящей в костномозговую полость эпифиза. Кровь в сосудах надкостницы поступает из нее наружу, средняя часть эпифиза в основном снабжается кровью из питающей артерии и лишь небольшое количество крови поступает в эпифиз из сосудов надкостницы. Если питающая артерия повреждается или перерезается при операции, то, возможно, что снабжение кровью эпифиза будет заменяться на питание из надкостницы, поскольку эти кровеносные сосуды взаимно связываются друг с другом при развитии плода.
Кровеносные сосуды в эпифизе проходят в него из боковых частей эпифизарной пластинки, развиваясь, превращаются в эпифизарные артерии, снабжающие кровью мозг эпифиза. Есть также большое количество ответвлений, снабжающих кровью хрящи вокруг эпифиза и его боковые части.
Верхняя часть кости представляет собой суставный хрящ, под которым находится эпифизарная артерия, а еще ниже ростовой хрящ, после чего имеются три вида кости: внутрихрящевая кость, костные пластинки и надкостница. Направление кровотока в этих трех видах кости неодинаково: во внутрихрящевой кости движение крови происходит вверх и наружу, в средней части диафиза сосуды имеют поперечное направление, а в нижней части диафиза сосуды направлены вниз и наружу. Поэтому кровеносные сосуды во всей плотной кости расположены в форме зонтика и расходятся лучеобразно.
Поскольку кровеносные сосуды в кости очень тонкие, и их невозможно наблюдать непосредственно, поэтому изучение динамики кровотока в них довольно затруднительно. В настоящее время с помощью радиоизотопов, внедряемых в кровеносные сосуды кости, судя по количеству их остатков и количеству выделяемого ими тепла в сопоставлении с пропорцией кровотока, можно измерить распределение температур в кости, чтобы определить состояние кровообращения.
В процессе лечения дегенеративно-дистрофических заболеваний суставов безоперационным методом в головке бедренной кости создается внутренняя электрохимическая среда, которая способствует восстановлению нарушенной микроциркуляции и активному удалению продуктов обмена разрушенных заболеванием тканей, стимулирует деление и дифференциацию костных клеток, постепенно замещающих дефект кости.
Плюсы и минусы костной пластики при имплантации
Конкурентные преимущества костной пластики:
- восстановление функций, даже если у пациента утрачен большое количество твердой ткани;
- нормализуется внешний вид десневой ткани и ротовой полости в целом;
- восстановление жевательных функций – все виды костной ткани в стоматологии адаптированы под большие нагрузки;
- возможность восстановить зубной ряд, даже в самых запущенных ситуациях.
Недостатки костной пластики:
- реабилитация занимает несколько месяцев;
- высок риск отторжения блока;
- болевые ощущения в процессе приживления тканей;
- немалая цена операции.
Причины атрофии
Такое заболевание образуется по вторичными причинам. Первичная дистрофия костей начинается еще в детском возрасте.
Первой причиной считается выпадение зубов. Она может быть толчком для начала атрофических процессов, или быть ее результатом. Биологически атрофия выглядит следующим образом – при отсутствии зуба его соседи теряют опору и начинают смещаться в пустое место. Это существенно увеличивает давление на альвеолу того зуба, который отсутствует. В результате разрушительные процессы начинают подавлять регенерацию.
Второй причиной является инволюция челюстей. В результате потери зубов с возрастом пластинки костей альвеол истончаются и исчезают. Кости из-за отсутствия стабильного внешнего давления замедляют функционирование остеобластов. А остеокласты наоборот активизируются. В результате с возрастом существенно понижается кровоснабжение ткани кости. И это оказывает негативное влияние на метаболизм ее клеток.
Третья причина заключается в системных патологиях. Тут большое значение отводится заболеваниям паращитовидных и щитовидных желез, ослаблению функции яичников. Все эти заболевания понижают в костях содержание гидроксиапатита. А это плохо сказывается на их прочностных характеристиках. Таким образом, для хорошего функционирования костей нужно чтобы регенерация преобладала над разрушением. Также причиной могут выступить хронические воспаления в костной ткани.
Четвертая причина состоит из давления зубного протеза. Здесь механический фактор играет главную роль. Однако, не все пациенты, которые долго носят зубные протезы, имеют рентгенологические доказательства снижения костной массы. Поэтому не все специалисты относят этот фактор к причинам атрофии.
Последствия атрофии
Данное заболевание может привести к определенным последствиям. Главное – это то, что станет невозможным закрепление имплантата и восстановление потерянных зубов. Кроме того, пациент может наблюдать и негативные перемены атрофии кости внешне, то есть меняется форма и вид лица, происходит нарушение функционирования многих органов.
Также атрофия костной ткани зубов может привести к:
- образованию мимических морщинок в зоне губ;
- необходимости проведения дополнительных манипуляций по увеличению костного объема перед тем, как провести имплантацию;
- невозможности пережевывания пищи, соответственно, это приводит к проблемам с желудочно-кишечным трактом;
- «западанию» внутрь губ;
- смещению в сторону зубов, в то место, где есть их отсутствие.
Кроме того, одним из важных последствий этого заболевания считают увеличение цены имплантации. Это объясняется тем, что для закрепления имплантатов потребуется определенный объем кости. Если его будет недостаточно, то нужно будет сделать его наращивание. А это подразумевает использование дополнительных материалов и лекарственных средств, работы специалиста.